3D-Bioprinted-Brustkrebsmodelle für verbesserte Medikamententests und Stoffwechselstudien:
Trotz Fortschritten bei der Modellierung der komplexen Tumormikroumgebung liefern herkömmliche Brustkrebsmodelle oft keine genauen Erkenntnisse über die Krebsbiologie und die Wirksamkeit von Medikamenten. Eine genaue Modellierung dieser Umgebung könnte die Wirksamkeit und Sicherheit von Krebsbehandlungen verbessern, indem genauere präklinische Modelle angeboten werden, die die In-vivo-Bedingungen nachahmen und Probleme wie Therapieresistenz und metabolische Vielfalt in Tumoren angehen.
Forscher der Semmelweis-Universität in Ungarn wollten ein 3D-Bioprint-Modell des menschlichen Brustkrebses entwickeln und bewerten, dass die in vivo-Umgebung des Tumors genau nachahmt. Dieses Modell soll im Vergleich zu herkömmlichen 2D-Kulturen und Xenotransplantaten eine präzisere Plattform für die Prüfung von Arzneimittelreaktionen und Stoffwechselzielen bieten.
Unter Verwendung einer Hydrogel-Bioink auf Alginatbasis druckten die Forscher 3D-Modelle von menschlichem Brustkrebs. Diese Modelle enthielten einen Kern aus Brustkrebszellen in einer gewebeähnlichen Struktur. Die biologisch gedruckten Modelle wurden langfristig kultiviert, um die Zellproliferation in vitro und die Wachstumskapazität und Kanzerogenität in vivo (in SCID-Mäusen) zu untersuchen.
Für die Erstellung der 3D-Modelle wurde der BioScaffolder 3.2 verwendet, um ihre Genauigkeit und Reproduzierbarkeit zu gewährleisten. Die Ergebnisse waren vielversprechend: Die 3D-Bioprint-Modelle zeigten im Vergleich zu 2D-Kulturen eine verbesserte Zellproliferation und kanzerogene Eigenschaften. Außerdem lieferten sie eine genauere Darstellung der Mikroumgebung des Tumors, was für wirksame Arzneimitteltests und Stoffwechselstudien entscheidend ist.
Durch die Verwendung von Hydrogelen auf Alginatbasis haben die Forscher gewebeähnliche Scaffolds geschaffen, die die Heterogenität und Medikamentenempfindlichkeit von tatsächlich in vivo wachsenden Brusttumoren nachbilden. Dieser Ansatz hat das Potenzial, die Notwendigkeit von Tierversuchen zu verringern und die Erfolgsquote klinischer Studien zu verbessern.
Die Studie kam zu dem Schluss, dass 3D-Bioprint-Brustkrebsmodelle eine realistischere und effektivere Plattform für das In-vitro-Targeting von Medikamenten und Stoffwechselprodukten bieten. Dieser Fortschritt könnte zu besseren präklinischen Tests führen und letztlich die Ergebnisse der Krebsbehandlung verbessern.
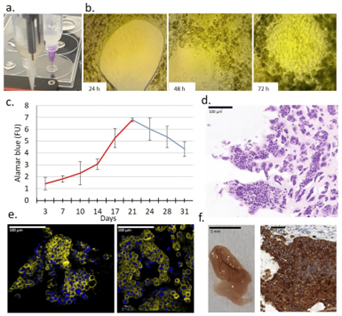
Teil von Abb. 3.: Charakteristik eines neuen bioprinted 3D-Gewebe- Modells von menschlichen Krebszellen ZR75.1. (a) Zwei einzeln betriebene Extruder für die Herstellung von 3D-bioprinted Strukturen für die Gewebemodellierung.
Dieser Artikel basiert auf der folgenden Veröffentlichung:
Dankó, T.; Petővári, G.; Raffay, R.; Sztankovics, D.; Moldvai, D.; Vetlényi, E.; Krencz, I.; Rókusz, A.; Sipos, K.; Visnovitz, T.; et al. Characterisation of 3D Bioprinted Human Breast Cancer Model for In Vitro Drug and Metabolic Targeting. Int. J. Mol. Sci. 2022, 23, 7444. https://doi.org/10.3390/ijms23137444
